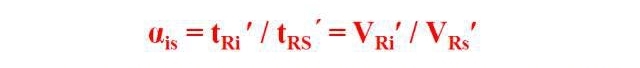hromatogrāfija, kas pazīstama arī kā "hromatogrāfiskā analīze", "hromatogrāfija", ir atdalīšanas un analīzes metode, kurai ir ļoti plašs pielietojums analītiskajā ķīmijā, organiskajā ķīmijā, bioķīmijā un citās jomās.
Hromatogrāfijas pamatlicējs ir krievu botāniķis M.Cveters.1906. gadā krievu botāniķis Zveters publicēja sava eksperimenta rezultātus: Lai atdalītu augu pigmentus, viņš stikla mēģenē ar kalcija karbonāta pulveri ielēja petrolētera ekstraktu, kas satur augu pigmentus, un eluēja to ar petrolēteri no augšas uz leju.Tā kā dažādiem pigmentiem ir atšķirīga adsorbcijas spēja uz kalcija karbonāta daļiņu virsmas, izskalošanās procesā dažādi pigmenti pārvietojas uz leju ar atšķirīgu ātrumu, tādējādi veidojot dažādu krāsu joslas.Pigmenta sastāvdaļas tika atdalītas.Viņš šo atdalīšanas metodi nosauca par hromatogrāfiju.
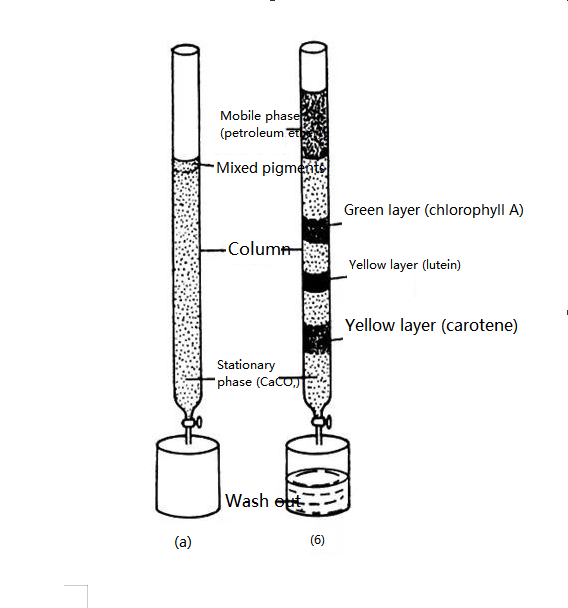
Augu lapu pigmenta atdalīšanas eksperimenta shematisks attēlojums
Nepārtraukti attīstoties atdalīšanas metodēm, par atdalīšanas objektu kļūst arvien vairāk bezkrāsainu vielu, arī hromatogrāfija pamazām zaudēja "krāsas" nozīmi, taču nosaukums tiek lietots vēl šodien.
Hromatogrāfiskā klasifikācija
Hromatogrāfijas būtība ir process, kurā atdalāmās molekulas tiek sadalītas un līdzsvarotas starp stacionāro fāzi un kustīgo fāzi.Dažādas vielas tiek sadalītas atšķirīgi starp abām fāzēm, kas liek tām pārvietoties ar dažādu ātrumu kopā ar mobilo fāzi.Kustīgās fāzes kustībā dažādas maisījuma sastāvdaļas tiek atdalītas viena no otras stacionārajā fāzē.Atkarībā no mehānisma to var iedalīt dažādās kategorijās.
1, saskaņā ar divfāžu fiziskā stāvokļa klasifikāciju
Mobilā fāze: gāzu hromatogrāfija, šķidruma hromatogrāfija, superkritiskā šķidruma hromatogrāfija
Stacionārā fāze: gāze-cieta, gāze-šķidrums;Šķidrums-ciets, šķidrums-šķidrums
2, atbilstoši stacionārās fāzes klasifikācijas formai
Kolonnu hromatogrāfija: pildītas kolonnas hromatogrāfija, kapilārās kolonnas hromatogrāfija, mikropakotās kolonnas hromatogrāfija, preparatīvā hromatogrāfija
Plaknes hromatogrāfija: papīra hromatogrāfija, plānslāņa hromatogrāfija, polimēru membrānas hromatogrāfija
3, klasificēts pēc atdalīšanas mehānisma
Adsorbcijas hromatogrāfija: dažādas sastāvdaļas tiek atdalītas atkarībā no to adsorbcijas un desorbcijas spējām uz adsorbentiem
Sadalījuma hromatogrāfija: dažādas sastāvdaļas atdala atkarībā no to šķīdības šķīdinātājā
Molekulārās izslēgšanas hromatogrāfija: atkarībā no atdalīšanas molekulārā izmēra lieluma jonu apmaiņas hromatogrāfija: dažādas afinitātes sastāvdaļas jonu apmaiņas sveķu atdalīšanai
Afinitātes hromatogrāfija: atdalīšana, izmantojot īpašu afinitāti starp bioloģiskām makromolekulām
Kapilārā elektroforēze: komponenti tika atdalīti atbilstoši mobilitātes un/vai nodalījuma uzvedības atšķirībām
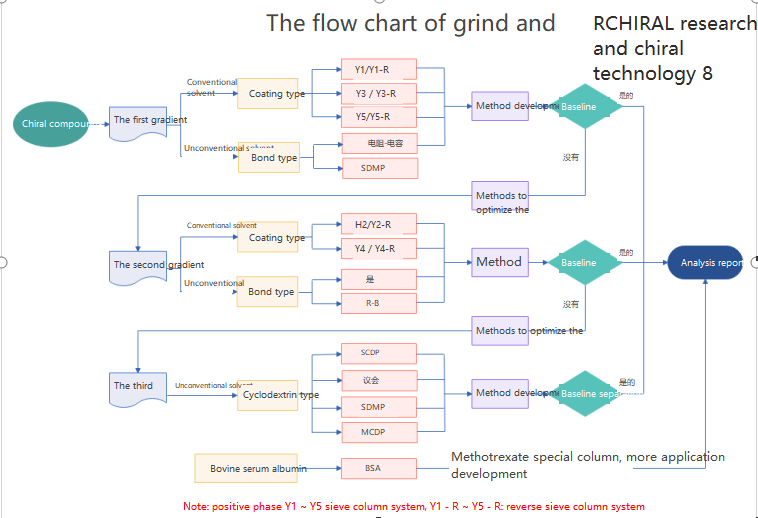
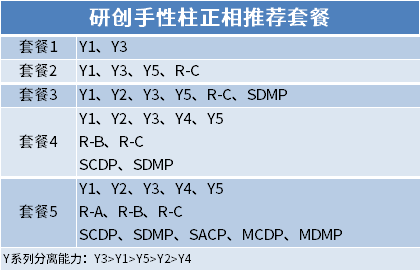
Hirālo hromatogrāfiju izmanto hirālo zāļu atdalīšanai un analīzei, kuras var iedalīt trīs kategorijās: hirālās atvasināšanas reaģenta metode;Hirālās mobilās fāzes piedevas metode;Hirālās stacionārās fāzes izšķirtspējas metode
Hromatogrāfijas pamatterminoloģija
Līknes, kas iegūtas, uzzīmējot komponentu atbildes signālus pēc hromatogrāfiskās atdalīšanas noteikšanas pret laiku, sauc par hromatogrammām.
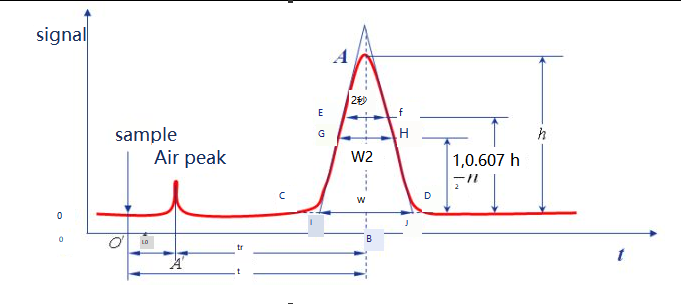
Pamatlīnija:Noteiktos hromatogrāfijas apstākļos signāla līkni, kas rodas, kad tikai kustīgā fāze iet caur detektoru sistēmu, sauc par bāzes līniju, kā parādīts ot rindā.Kad eksperimentālais stāvoklis bija stabils, bāzes līnija bija līnija, kas ir paralēla horizontālajai asij.Bāzes līnija atspoguļo instrumenta, galvenokārt detektora, radīto troksni laika gaitā.
Pīķa augstums:vertikālais attālums starp hromatogrāfijas pīķa punktu un bāzes līniju, ko apzīmē ar h, kā parādīts AB līnijā.
Reģiona platums:Hromatogrāfiskā pīķa apgabala platums ir tieši saistīts ar atdalīšanas efektivitāti.Ir trīs metodes, lai aprakstītu hromatogrāfiskā pīķa platumu: standarta novirze σ, pīķa platums W un FWHM W1/2.
Standarta novirze (σ):σ ir puse attāluma starp diviem lēciena punktiem normālā sadalījuma līknē, un σ vērtība norāda komponentu izkliedes pakāpi prom no kolonnas.Jo lielāka ir σ vērtība, jo izkliedētākas ir notekūdeņu sastāvdaļas un sliktāks atdalīšanas efekts.Un otrādi, notekūdeņu komponenti ir koncentrēti, un atdalīšanas efekts ir labs.
Pīķa platums W:Krustošanās punkti abās hromatogrāfiskās pīķa pusēs tiek izmantoti kā pieskares līnijas, un bāzes līnijas krustpunktu sauc par pīķa platumu vai bāzes līnijas platumu, ko var izteikt arī kā W, kā parādīts IJ attēlā.Saskaņā ar normālā sadalījuma principu var pierādīt, ka sakarība starp pīķa platumu un standartnovirzi ir W=4σ.
W1/2:Pīķa platumu pie puse no pīķa augstuma sauc par FWHM, kā parādīts GH attālumam.W1/2=2,355σ, W=1,699 W1/2.
W1/2, W ir atvasināti no σ un tiek izmantoti, lai aprēķinātu pīķu laukumus papildus kolonnas efekta mērīšanai.FWHM mērīšana ir ērtāka un visbiežāk izmantota.
īss kopsavilkums
No hromatogrāfiskās maksimālās izplūdes līknes var sasniegt šādus mērķus:
a, Kvalitatīva analīze tika veikta, pamatojoties uz hromatogrāfisko pīķu aiztures vērtību
b, kvantitatīvā analīze, pamatojoties uz hromatogrāfiskās pīķa laukumu vai maksimumu
C. Kolonnas atdalīšanas efektivitāte tika novērtēta pēc aiztures vērtības un hromatogrāfiskās pīķa pīķa platuma
Hromatogrāfijā izmantotā aprēķina formula
1. Saglabāšanas vērtība
Aiztures vērtība ir parametrs, ko izmanto, lai aprakstītu pakāpi, kādā parauga komponents tiek saglabāts kolonnā, un tiek izmantots kā hromatogrāfiskā raksturojuma indikators.Tās attēlošanas metode ir šāda:
Aiztures laiks tR
Nāves laikstM
Pielāgojiet aiztures laiku tR'=tR-tM
(Kopējais laiks, kas pavadīts stacionārā fāzē)
Saglabāšanas apjoms
VR=tR*F. (neatkarīgs no kustīgās fāzes ātruma)
Mirušais apjoms
VM=tM*Fc
(Telpa, ko neaizņem stacionārā fāze plūsmas ceļā no inžektora uz detektoru)
Pielāgojiet saglabāšanas skaļumu VR'=t'R*Fc
2. Relatīvā saglabāšanas vērtība
Relatīvā aiztures vērtība, kas pazīstama arī kā atdalīšanas koeficients, sadalījuma koeficienta koeficients vai relatīvās jaudas koeficients, ir pārbaudītā komponenta koriģētā aiztures laika (tilpuma) attiecība pret standarta koriģēto aiztures laiku (tilpumu) noteiktos hromatogrāfijas apstākļos.

Relatīvās aiztures vērtības tika izmantotas, lai novērstu noteiktu darbības apstākļu, piemēram, plūsmas ātruma un fiksācijas zudumu, ietekmi uz aiztures vērtībām.Relatīvās aiztures vērtības standarts var būt pārbaudītā parauga sastāvdaļa vai mākslīgi pievienots savienojums.
3. Saglabāšanas indekss
Aiztures indekss ir testējamās vielas i aiztures indekss fiksētā šķīdumā X. Par standartvielām izvēlas divas n-alēnas, no kurām vienai ir N oglekļa atomu skaits, bet otrai ir N+n.To koriģētais aiztures laiks ir attiecīgi t'r (N) un t'r (N+n), lai pārbaudāmās vielas i pielāgotais aiztures laiks t 'r (i) būtu tieši starp tiem, tas ir, t'r (N).
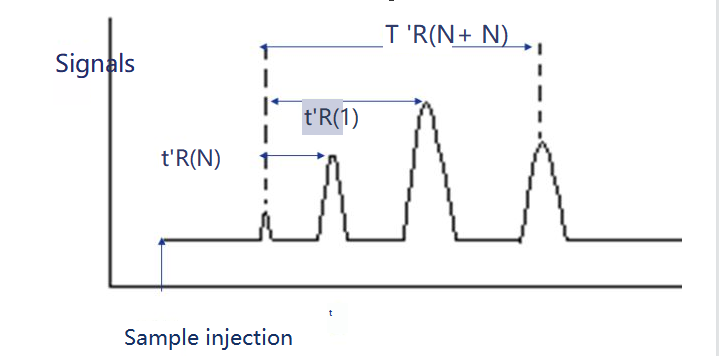
Saglabāšanas indeksu var aprēķināt šādi.
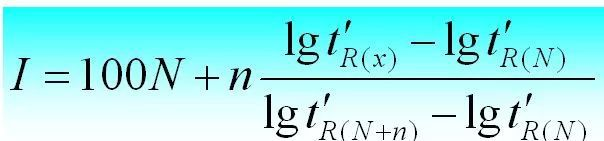
4. Jaudas koeficients (k)
Līdzsvara stāvoklī komponenta masas attiecība stacionārajā fāzē (-ēs) pret kustīgo fāzi (m), ko sauc par kapacitātes koeficientu.Formula ir šāda:
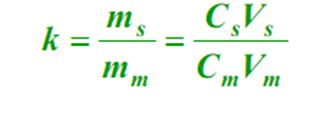
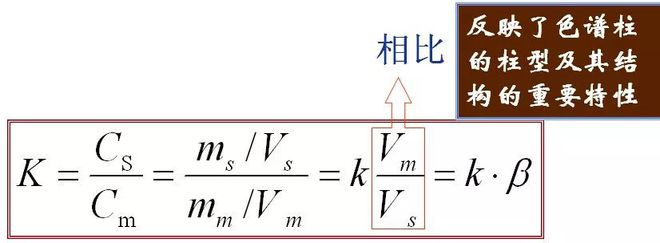
5. Sadalījuma koeficients (K) Līdzsvarā komponenta koncentrācijas attiecība stacionārajā fāzē (-ēs) pret kustīgo fāzi (m), ko sauc par sadalījuma koeficientu.Formula ir šāda

Attiecība starp K un k:
Tas atspoguļo kolonnas tipu un tā mezgla svarīgās struktūras īpašības
īss kopsavilkums
Saistība starp saglabāšanas vērtību un jaudas koeficientu un sadalījuma koeficientu:
Hromatogrāfiskā atdalīšana balstās uz katra komponenta adsorbcijas vai šķīdināšanas spēju atšķirību fiksētā relatīvā paraugā, ko var kvantitatīvi izteikt ar sadalījuma koeficienta K (vai kapacitātes koeficienta k) lielumu.
Komponentiem ar spēcīgu adsorbcijas vai šķīdināšanas spēju ir liels sadalījuma koeficients (vai kapacitātes koeficients) un ilgs aiztures laiks.Un otrādi, komponentiem ar vāju adsorbciju vai šķīdību ir mazs sadalījuma koeficients un īss aiztures laiks.
Hromatogrāfijas pamatteorija
1. Paplātes teorija
(1) Izvirzīts - termodinamiskā teorija
Tas sākās ar torņa plāksnes modeli, ko piedāvāja Martin un Synge.
Frakcionēšanas kolonna: paplātē vairākas reizes gāzes un šķidruma līdzsvara nodrošināšanai atkarībā no viršanas temperatūras dažādās atdalīšanas vietās.
Kolonna: komponenti ir līdzsvaroti ar vairākām starpsienām starp abām fāzēm un atdalīti atbilstoši dažādiem sadalījuma koeficientiem.
(2) Hipotēze
(1) Kolonnā ir daudz paplātes, un komponenti var ātri sasniegt sadalījuma līdzsvaru paplātes intervālā (tas ir, paplātes augstumā).
(2) Kustīgā fāze ieiet kolonnā, nevis nepārtraukti, bet pulsējot, tas ir, katra eja ir kolonnas tilpums.
(3) Kad paraugs tika pievienots katrai kolonnas plāksnei, parauga difūziju pa kolonnas asi varēja neņemt vērā.
(4) Sadalījuma koeficients ir vienāds uz visām paplātēm neatkarīgi no komponentu daudzuma.Tas nozīmē, ka sadalījuma koeficients ir nemainīgs katrā tabanā.
(3) Princips
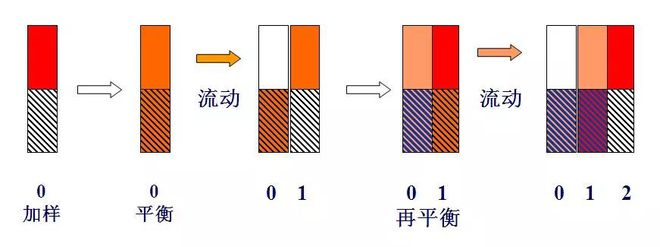
Paplātes teorijas shematiskā diagramma
Ja 0. paplātei pievieno masas vienības sastāvdaļu, proti, m=1 (piemēram, 1mg vai 1μg), un pēc sadalījuma līdzsvara, jo k=1, proti, ns=nm, nm=ns=0.5.
Kad nesējgāzes plāksnes tilpums (lΔV) pulsācijas veidā nonāk plāksnē 0, nesējgāze, kas satur nm komponentu gāzes fāzē, tiek nospiesta uz 1. plāksni. Šajā laikā ns komponents plāksnes 0 šķidrajā fāzē. un nm komponents 1. plāksnes gāzes fāzē tiks pārdalīts starp abām fāzēm.Līdz ar to 0. plāksnītes kopējais komponentu daudzums ir 0,5, kurā gāzes un šķidruma fāze ir katra 0,25, un kopējais 1. plāksnītes saturs arī ir 0,5.Gāzes un šķidruma fāzes arī bija 0,25.
Šo procesu atkārto katru reizi, kad kolonnā tiek pulsēta jauna plāksnes tilpuma nesējgāze (skatīt tabulu zemāk).
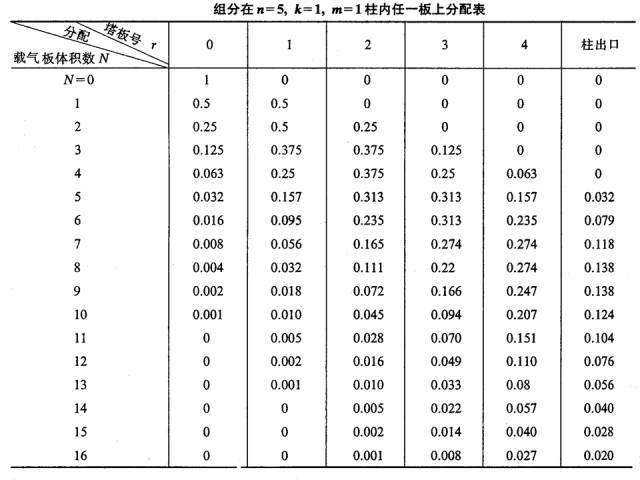
(4) Hromatogrāfiskās izplūdes līknes vienādojums

σ ir standarta novirze, ir aiztures laiks, C ir koncentrācija jebkurā laikā,
C ir injekcijas koncentrācija, tas ir, kopējais komponentu daudzums (pīķa laukums A).
(5) kolonnas efektivitātes parametri
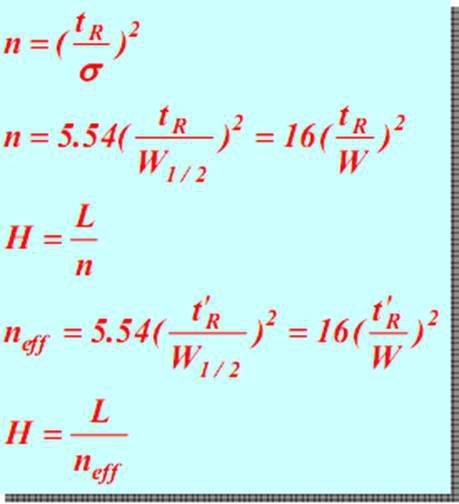
Pie nemainīgas tR, jo mazāks W vai w 1/2 (tas ir, jo šaurāks maksimums), jo lielāks ir teorētisko plākšņu skaits n, jo mazāks ir teorētiskais plāksnes augstums un augstāka kolonnas atdalīšanas efektivitāte.Tas pats attiecas uz efektīvas teorijas paplāti neff.Tāpēc teorētiskais paplāšu skaits ir rādītājs, lai novērtētu kolonnu efektivitāti.
(5)Pazīmes un trūkumi
> Priekšrocības
Paplātes teorija ir daļēji empīriska un izskaidro izplūdes līknes formu
Ir ilustrēti komponentu sadalīšanas un atdalīšanas procesi
Tiek piedāvāts rādītājs kolonnas efektivitātes novērtēšanai
> Ierobežojumi
Komponenti nevar īsti sasniegt sadalījuma līdzsvaru divās fāzēs:
Nevar ignorēt komponentu garenisko difūziju kolonnā:
Dažādu kinētisko faktoru ietekme uz masas pārneses procesu netika ņemta vērā.
Sakarību starp kolonnas efektu un kustīgās fāzes plūsmas ātrumu nevar izskaidrot:
Nav skaidrs, kādi galvenie faktori ietekmē kolonnas efektu
Šīs problēmas ir apmierinoši atrisinātas likmju teorijā.
2. Likmes teorija
1956. gadā holandiešu zinātnieks VanDēmters u.c.absorbēja paplātes teorijas jēdzienu un apvienoja kinētiskos faktorus, kas ietekmē paplātes augstumu, izvirzīja hromatogrāfijas procesa kinētisko teoriju - ātruma teoriju un atvasināja VanDēmtera vienādojumu.Tajā hromatogrāfiskais process tiek uzskatīts par dinamisku nelīdzsvara procesu un pētīta kinētisko faktoru ietekme uz pīķa paplašināšanos (ti, kolonnas efektu).
Vēlāk Giddings un Snyder et al.ierosināja šķidruma hromatogrāfijas ātruma vienādojumu (proti, Gidingsa vienādojumu), pamatojoties uz VanDeemter vienādojumu (vēlāk saukts par gāzu hromatogrāfijas ātruma vienādojumu) un saskaņā ar īpašību starpību starp šķidrumu un gāzi.
(1) Van Dēmtera vienādojums
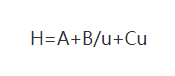
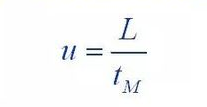
Kur: H: ir dēļa augstums
A: virpuļdifūzijas koeficients
B: molekulārās difūzijas termiņa koeficients
C: masas pārneses pretestības termiņa koeficients
(2) Gidingsa vienādojums
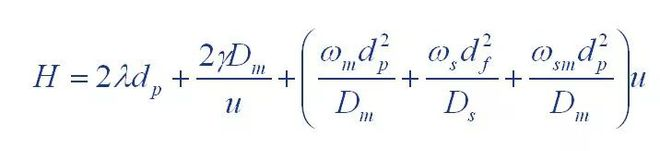
Kvantitatīvā un kvalitatīvā analīze
(1) Kvalitatīva analīze
Kvalitatīvā hromatogrāfiskā analīze ir paredzēta, lai noteiktu savienojumus, ko attēlo katrs hromatogrāfiskais maksimums.Tā kā dažādām vielām noteiktos hromatogrāfijas apstākļos ir noteiktas aiztures vērtības, aiztures vērtību var izmantot kā kvalitatīvu indeksu.Uz aiztures vērtībām pašlaik balstās dažādas hromatogrāfijas kvalitatīvās metodes.
Tomēr dažādām vielām var būt līdzīgas vai identiskas aiztures vērtības vienādos hromatogrāfijas apstākļos, tas ir, aiztures vērtības nav izslēdzošas.Tādējādi ir grūti raksturot pilnīgi nezināmu paraugu, pamatojoties tikai uz saglabāšanas vērtībām.Ja, pamatojoties uz izpratni par parauga avotu, raksturu un mērķi, var izdarīt iepriekšēju spriedumu par parauga sastāvu, un var izmantot šādas metodes, lai noteiktu savienojumu, ko attēlo hromatogrāfiskā pīķa.
1. Kvalitatīva kontrole, izmantojot tīras vielas
Noteiktos hromatogrāfijas apstākļos nezināmajam ir tikai noteikts aiztures laiks.Tāpēc nezināmo var kvalitatīvi identificēt, salīdzinot zināmās tīrās vielas aiztures laiku tādos pašos hromatogrāfijas apstākļos ar nezināmas vielas aiztures laiku.Ja abas ir vienādas, nezināmā viela var būt zināma tīra viela;Citādi nezināmais nav tīrā viela.
Tīras vielas kontroles metode ir piemērojama tikai nezināmai vielai, kuras sastāvs ir zināms, kuras sastāvs ir salīdzinoši vienkāršs un kuras tīrā viela ir zināma.
2. Relatīvās saglabāšanas vērtības metode
Relatīvā aiztures vērtība α attiecas uz pielāgošanu starp komponentu i un atsauces materiāliem. Aiztures vērtību attiecība:
Tas mainās tikai, mainoties fiksatora un kolonnas temperatūrai, un tam nav nekāda sakara ar citiem darbības apstākļiem.
Pie noteiktas stacionārās fāzes un kolonnas temperatūras attiecīgi mēra komponenta i un standartvielas s koriģētās aiztures vērtības un pēc tam aprēķina saskaņā ar iepriekš minēto formulu.Iegūtās relatīvās aiztures vērtības var kvalitatīvi salīdzināt ar atbilstošajām vērtībām literatūrā.
3, pievienojot zināmas vielas, lai palielinātu pīķa augstuma metodi
Ja nezināmajā paraugā ir daudz komponentu, iegūtie hromatogrāfiskie pīķi ir pārāk blīvi, lai tos varētu viegli identificēt ar iepriekš minēto metodi, vai ja nezināmais paraugs tiek izmantots tikai norādītā vienuma analīzei.
"Vispirms tiek izveidota nezināma parauga hromatogramma, un pēc tam tiek iegūta papildu hromatogramma, nezināmam paraugam pievienojot zināmu vielu."Šādām vielām var būt zināmas sastāvdaļas ar palielinātu pīķu augstumu.
4. Saglabājiet indeksa kvalitatīvo metodi
Aiztures indekss atspoguļo vielu aiztures uzvedību uz fiksatoriem un pašlaik ir visplašāk izmantotais un starptautiski atzītais kvalitatīvais indekss GC.Tam ir labas reproducējamības, vienota standarta un maza temperatūras koeficienta priekšrocības.
Aiztures indekss ir saistīts tikai ar stacionārās fāzes īpašībām un kolonnas temperatūru, bet ne ar citiem eksperimenta apstākļiem.Tās precizitāte un reproducējamība ir lieliska.Kamēr kolonnas temperatūra ir tāda pati kā stacionārajai fāzei, identifikācijai var izmantot literatūras vērtību, un salīdzināšanai nav nepieciešams izmantot tīru materiālu.
(2) Kvantitatīvā analīze
Hromatogrāfiskās kvantitatīvās noteikšanas pamats:
Kvantitatīvās analīzes uzdevums ir atrast simts komponentu jauktajā paraugā
Daļējs saturs.Hromatogrāfiskā kvantitatīvā noteikšana balstījās uz sekojošo: ja darbības apstākļi bija konsekventi, bija
Mērītās sastāvdaļas masu (vai koncentrāciju) nosaka detektora sniegtais atbildes signāls
Tas ir proporcionāli.Proti:
Hromatogrāfiskās kvantitatīvās noteikšanas pamats:
Kvantitatīvās analīzes uzdevums ir atrast simts komponentu jauktajā paraugā
Daļējs saturs.Hromatogrāfiskā kvantitatīvā noteikšana balstījās uz sekojošo: ja darbības apstākļi bija konsekventi, bija
Mērītās sastāvdaļas masu (vai koncentrāciju) nosaka detektora sniegtais atbildes signāls
Tas ir proporcionāli.Proti:
1. Pīķa laukuma mērīšanas metode
Pīķa laukums ir pamata kvantitatīvie dati, ko nodrošina hromatogrammas, un pīķa laukuma mērījumu precizitāte tieši ietekmē kvantitatīvos rezultātus.Dažādas mērīšanas metodes tika izmantotas hromatogrāfijas pīķiem ar dažādu pīķu formu.
Kvantitatīvā analīzē ir grūti atrast precīzu ziemas vērtību:
No vienas puses, sakarā ar grūtībām precīzi izmērīt absolūto injekcijas tilpumu: no otras puses
Pīķa laukums ir atkarīgs no hromatogrāfijas apstākļiem, un hromatogrāfijas josla ir jāsaglabā, kad tiek mērīta vērtība
To pašu darīt nav ne iespējams, ne ērti.Un pat ja jūs to varat izdarīt pareizi
Precīza vērtība arī tāpēc, ka nav vienota standarta un to nevar tieši piemērot.
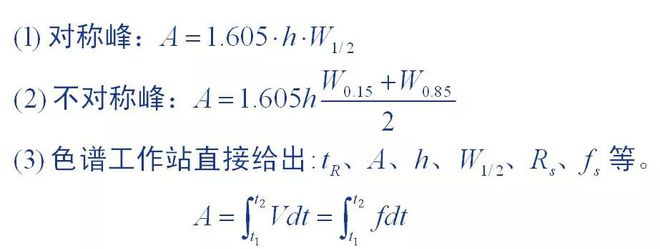
2.Kvantitatīvās korekcijas koeficients
Kvantitatīvās korekcijas koeficienta definīcija: komponentu daudzums, kas nonāk detektorā (m)
Tā hromatogrāfiskā pīķa laukuma (A) vai pīķa augstuma () attiecība ir proporcionalitātes konstante (,
Proporcionalitātes konstanti sauc par komponenta absolūto korekcijas koeficientu.
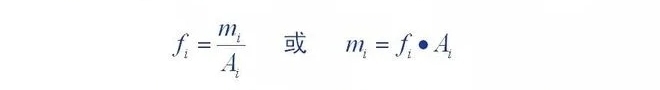
Kvantitatīvā analīzē ir grūti atrast precīzu ziemas vērtību:
No vienas puses, sakarā ar grūtībām precīzi izmērīt absolūto injekcijas tilpumu: no otras puses
Pīķa laukums ir atkarīgs no hromatogrāfijas apstākļiem, un hromatogrāfijas josla ir jāsaglabā, kad tiek mērīta vērtība
To pašu darīt nav ne iespējams, ne ērti.Un pat ja jūs to varat izdarīt pareizi
Precīza vērtība arī tāpēc, ka nav vienota standarta un to nevar tieši piemērot.
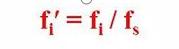
Tas nozīmē, ka komponenta relatīvais korekcijas koeficients ir komponents un atsauces materiāls s
Absolūto korekcijas koeficientu attiecība.
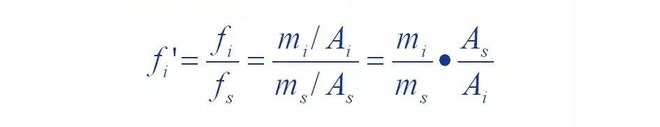
Var redzēt, ka relatīvais korekcijas koeficients ir tad, kad komponenta kvalitāte pret standartu.
Ja viela s ir vienāda, atsauces materiāla pīķa laukums ir komponenta pīķa laukums
Vairāki.Ja kādai sastāvdaļai ir masa m un pīķa laukums A, tad f'A skaits
Vērtības ir vienādas ar atsauces materiāla pīķa laukumu ar masu.Citiem vārdiem sakot,
Izmantojot relatīvo korekcijas koeficientu, var atdalīt katra komponenta pīķu laukumus
Pārvērš par atsauces materiāla pīķa laukumu, kas vienāds ar tā masu, pēc tam attiecību
Standarts ir vienots.Tātad šī ir normalizētā metode katra komponenta procentuālās daļas noteikšanai
Daudzuma pamats.
Relatīvās korekcijas koeficienta iegūšanas metode: relatīvās korekcijas koeficienta vērtības tika salīdzinātas tikai ar būtību
Mērījums ir saistīts ar standartu un detektora tipu, bet ar darbības joslu
Tas nav svarīgi.Tāpēc vērtības var iegūt no atsaucēm literatūrā.Ja teksts
Ja piedāvājumā nevarat atrast vēlamo vērtību, varat to noteikt arī pats.Noteikšanas metode
Metode: Noteikts daudzums izmērītās vielas desmit izvēlēts references materiāls → izveidots noteiktā koncentrācijā
Tika izmērīti abu komponentu hromatogrāfiskie pīķu laukumi A un As.
Tāda ir formula.
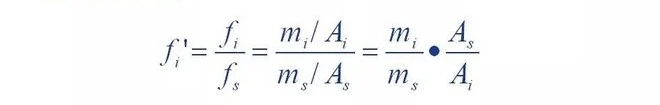
3. Kvantitatīvā aprēķina metode
(1) Platības normalizācijas metode
Visu bezpīķu frakciju satura summa kvantitatīvai noteikšanai tika aprēķināta kā 100%.
Šo metodi sauc par normalizāciju.Tās aprēķina formula ir šāda:
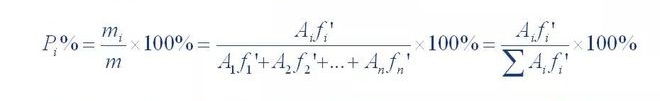
kur P,% ir pārbaudīto komponentu procentuālais saturs;A1, A2... A n ir 1. komponents. Pīķa laukums 1~n;f'1, f'2... f'n ir relatīvais korekcijas koeficients komponentiem no 1 līdz n.
(2) ārējā standarta metode
Kvantitatīvās salīdzināšanas metode starp paraugā pārbaudāmā komponenta atbildes signālu un tīro komponentu, kas pārbaudāms kā kontrole.
(3) Iekšējā standarta metode
Tā sauktā iekšējā standarta metode ir metode, kurā pārbaudāmās vielas standartšķīdumam un parauga šķīdumam kā iekšējam standartam pievieno noteiktu daudzumu tīras vielas, pēc tam analizē un nosaka.
(3) standarta pievienošanas metode
Standarta pievienošanas metode, kas pazīstama arī kā iekšējā pievienošanas metode, ir pievienot noteiktu daudzumu (△C)
Pārbaudāmajam parauga šķīdumam pievienoja testējamās vielas atsauci, un testu pievienoja testam
Parauga šķīduma maksimums pēc vielas bija augstāks nekā sākotnējā parauga šķīdumā
Lai aprēķinātu vielas koncentrāciju parauga šķīdumā, tika izmantots laukuma pieaugums (△A).
Saturs (Cx)
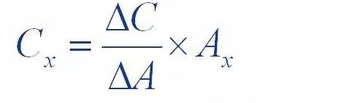
Kur Ax ir sākotnējā paraugā izmērāmās vielas pīķa laukums.

Izlikšanas laiks: 27-2023. marts